基于生物亲和性的生物分析(如免疫分析和核酸检测)方法学在很大程度上依赖于标记技术。在小分子标记技术中,产生信号的单元通过共价键被连接至可与测定程序中的被测物特异性结合的生物分子的某些功能基团上。在一些竞争性的分析方法中,产生信号的单元通过共价键被连接在被测物分子上后,与样本中的被测物竞争其特异性结合物。在传统的临床电化学发光(Electrochemiluminescence,ECL)免疫分析中作为标记分子的是一种三联吡啶钌 (II) 的活性酯,如[4-(N-琥珀酰亚胺基-氧羰基丙基)-4´-甲基-2,2´-联吡啶]双-(2,2´-联吡啶) 钌 (II) 的六氟磷酸盐。在发光基团三联吡啶钌[Ru(bpy)3]2+和共反应剂三正丙胺(TPA)经历电化学氧化和一系列下游化学反应后,形成发光激发态 [Ru(bpy)3]2+*,并发出可检测的光。ECL免疫分析涉及到抗体(在夹心法中)或被测物(在竞争法中)如何被标记,被测物如何被捕获,ECL反应如何被触发以及工作电极如何再生等诸多技术细节。以ECL夹心法免疫分析为例,在一个典型的ECL分析中,用多个[Ru(bpy)3]2+发光基团在被测物的一个特异性抗体(信号抗体)的赖氨酸残基的侧链氨基位点处标记抗体,而另一个抗体(捕获抗体)被生物素化。当一个临床样本与这两类抗体以及链霉亲和素包裹的磁微珠按预设的比例和时间互相混合后,一种夹心结构免疫复合体就在磁微珠表面形成。然后,磁微珠被带入一个电化学发光测量池(流动池)并被位于测量池下的可移动磁铁捕获在电化学工作电极表面。含三丙胺的缓冲溶液冲洗掉不需要的物质并提供一种可使 TPA 和 [Ru(bpy)3]2+发光基团经历以下反应 (1)-(5) 的化学环境。
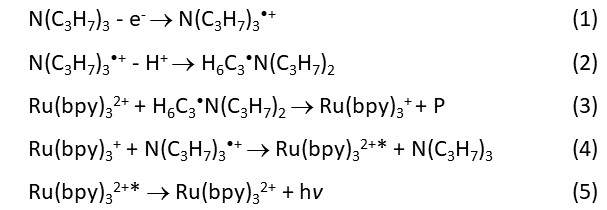
导致激发态[Ru(bpy)3]2+*的形成和ECL的产生的反应路径可能有多个(见 J. K. Leland and M. J. Powell, J. Electrochem. Soc. 1990, 137, 3127-3131, and W. Miao, J.-P. Choi, A. J. Bard, J. Am. Chem. Soc. 2002, 124, 14478-14485)。 某些机理可能只在均相溶液中起作用,但不能支持在微米级的磁珠绝大部分表面上[Ru(bpy)3]2+的电氧化。
不同于其它化学发光过程,三联吡啶钌在发光过程中只经历氧化还原状态的变化,即:
[Ru(bpy)3]2+ → [Ru(bpy)3]+ → [Ru(bpy)3]2+* → [Ru(bpy)3]2+,
而本身不被消耗,因此,在三丙胺大大过量时,其发光可以持续很长时间,直到停止施加电压。对一定时间段发出的光进行积分,可以得到 ECL 的相对光强测试值 RLU (RelativeLight Unit)。在含 [Ru(bpy)3]2+ 和三丙胺的均相缓冲溶液中,指定某特定浓度的 [Ru(bpy)3]2+ 的发光值后,其它浓度的发光值具有很好的线性关系。但在ECL免疫分析中,发光值和被测物浓度的关系在大范围内是非线性的, 通常用四参数 Logistic 函数拟合ECL信号和浓度的关系。
激发态[Ru(bpy)3]2+*在不同的缓冲溶液中可能经历不同的反应 (见顶图*), 使得ECL反应体系很复杂。优化ECL的产生过程 - 尤其是通过控制这些过程来获得优异的 ECL 免疫分析性能指标 - 需要化学和电化学领域的长期技术和经验积累。
* 安赛诊断鼓励相关机构或个人在尊重安赛诊断著作权 (著作权登记号:国作登字-2021-L-00219859) 的前提下使用本页面的 "三联吡啶钌的不同氧化态和激发态可能经历的化学反应" 和 "三联吡啶钌的电化学发光随时间的衰减及其浓度响应" 等图。如有出版需要,安赛诊断乐于提供免费使用的书面许可。